Tidak dapat menerangkan pengaruh medan magnet. Teori atom Bohr memiliki beberapa kelemahan yaitu teori ini hanya mampu menerangkann spektrum dari atom atau ion yang memiliki satu elektron sehingga tidak sesuai untuk spektrum atom atau ion yang memiliki elektron lebih dari satu serta tidak mampu menerangkan bagaimana terjadinya ikatan kimia saat atom membentuk molekul.

Teori Atom Menurut J J Thomson 1 Atom Berbentuk Bola Pejal Yang Bermuatan Positif Dan Tersebar Muatan Negatif Yang Merata Diseluruh Teori Rumus Kimia Kimia
Tidak dapat menjelaskan adanya ketidakpastian Heisenberg atau tidak dapat menerangkan kedudukan elektron dengan pasti.
Teori atom niels bohr memiliki kelemahan yaitu. Teori Atom Niels Bohr memiliki kelemahan yaitu. Tidak dapat menjelaskan spektrum unsurhalogenB. Kelemahan Teori Atom Bohr Itu melanggar Prinsip Ketidakpastian Heisenberg.
Ini termasuk masalah yang timbul dari mekanika klasik yang meramalkan bahwa elektron akan melepaskan radiasi elektromagnetik sambil mengorbit nukleus. Tidak dapat menentukan posisi elektrondengan pastiD. Tidak dapat menentukan posisi elektron dengan pasti.
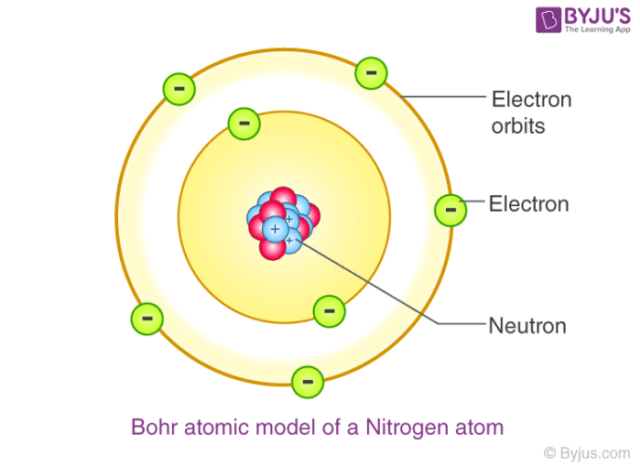
Salah satunya mengenai atom dimana teori tentang atom ini telah ada sejak beberapa abad sebelum masehi dan terus diteliti dengan berbagai eksperimen oleh para ilmuwan. Model atom Bohr dinyatakan dengan dua postulat 1. Teori atom Niels Bohr memiliki kelemahan yaitu.
Tidak dapat menentukan perubahan. Gagasan Bohr menyatakan bahwa elektron harus mengorbit di sekeliling inti. Sebab memiliki radius dan orbit yang bertentangan atau tidak sesuai dengan Prinsip Ketidakpastian Heisenberg.
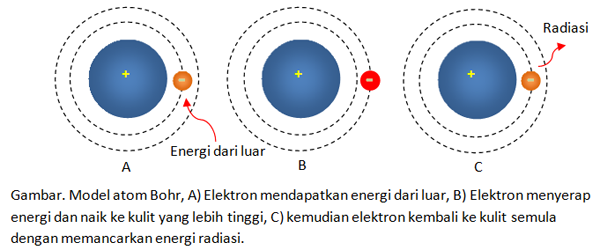
Elektron akan menyerap energi jika berpindah ke orbit yang lebih luar dan akan membebaskan energi jika berpindah ke orbit yang lebih. Model atom Bohr hanya secara tepat menjelaskan garis spektrum atom plaing sederhana yaitu atom Hidrogen yang hanya terdiri atas satu proton di intinya dan satu elektron saja. Bertentangan dengan hukum-hukum fisika klasik dari Maxwell.
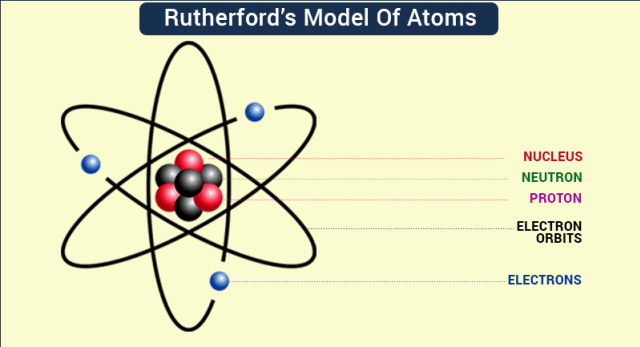
Kelemahan teori atom Rutherford yang diperbaiki oleh Neils Bohr yaitu. Untuk menutupi kelemahan model atom Rutherford Bohr mengeluarkan empat postulat. Teori Atom Bohr memperbaiki beberapa elemen model Rutherford yang bermasalah.
Kelemahan teori atom Rutherford diperbaiki oleh Neils Bohr. Bertentangan dengan teori atom Dalton bahwa atom-atom suatu unsur identik. Kejadian dalam ikatan kimia tidak dapat diterangkan.
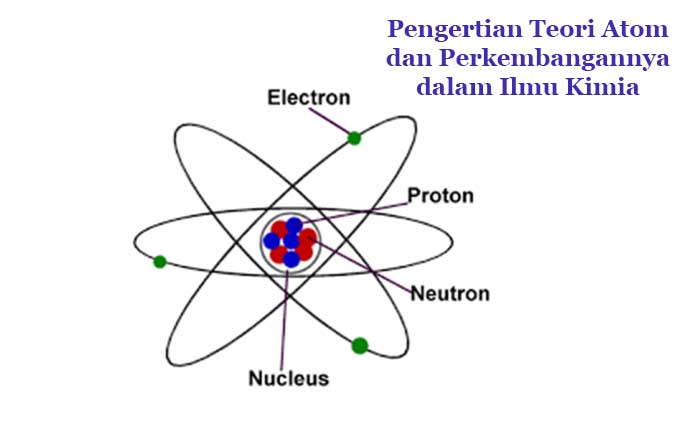
Atom tersusun dari inti atom yang bermuatan positif dan elektron bermuatan negatif. Kelemahan Teori Atom Bohr Secara ringkas kelemahan teori atom bohr yaitu. Pada tahun Niels Bohr mengoreksi kelemahan teori atom Rutherford dengan teori kuantum Planck.
Tramwayniceix dan 878 orang menganggap jawaban ini membantu. Teori model atom Bohr menganggap elektron memiliki radius dan orbit yang diketahui yaitu posisi dan momentum yang diketahui pada saat yang sama yang tidak mungkin menurut Heisenberg. Berkembangnya ilmu pengetahuan dari waktu ke waktu memberikan pengaruh terhadap peradaban manusia.
Hanya saja teori atom yang dikemukakan Bohr kemudian memiliki kelemahan. Model atom Bohr memperbaiki kelemahan model atom Rutherford. Teori atom Niels Bohr memiliki kelemahan yaitu A.
Model atom Bohr dinyatakan dengan dua postulat 1. -Kelemahan Teori Atom Niels Bohr i penyimpangan untuk atom yang lebih besar daripada hidrogen. A memiliki arti tidak dan tomos memiliki arti dibagi.
Elektron-elektron yang mengelilingi inti mempunyai lintasan dan energi tertentu. Berlaku untuk partikel makroskopik. Atom jika berdasarkan bahasa Yunani yaitu atomos.
Baca juga Sel Volta. Prinsip tersebut menyatakan bahwa di dalam radius tidak akan dijumpai adanya orbit. Namun demikian teori atom yang dikemukakan oleh Neils Bohr juga memiliki banyak kelemahan.
Sedangkan untuk atom lebih besar yang memiliki banyak elektron dan proton model atom Bohr tidak cocok. Karena kehilangan energi elektron seharusnya dengan cepat berputar ke dalam dan runtuh dalam nukleus. Model atom Bohr didasarkan pada spektrum atom dan juga Mekanika Newton ini yang berlaku untuk benda-benda makroskopik bukan untuk partikel mikroskopis.
Memahami Teori Atom Bohr. Bertentangan dengan hukum-hukum fisikaklasik dari MaxwellC. Niels Henrik David Bohr menyempurnakan teori atom sebelum sebelumnya yang sudah ada teori atom Bohr menjelaskan sebagai berikut.
Tidak dapat menjelaskan spektrum unsur halogen. Bertentangan dengan hukum-hukum fisika klasik dari maxwell. Bertentangan dengan teori atom Dalton bahwa atom-atom suatu unsur identik.
Bertentangan dengan teori atom Daltonbahwa atom-atom suatu unsur identikE. Kelemahan teori atom Rutherford diperbaiki oleh Neils Bohr. Tidak dapat menerangkan efek Zeeman yaitu.
Tidak dapat menentukan perubahan energipada perpindahan elektron dalam atom. Tidak dapat menentukan posisi elektron dengan pasti. Pada tahun Niels Bohr mengoreksi kelemahan teori atom Rutherford dengan teori kuantum Planck.
Kelemahan teori atom Rutherford yang tidak dapat menjelaskan pengaruh gaya tarik elektrostatik elektron yang bermuatan negatif dan inti atom yang bermuatan positif akhirnya terjawab melalui serangkaian analisis yang dilakukan oleh ilmuwan bernama Niels Bohr. Tidak dapat menerangkan efek Zeeman yaitu. Dalam orbital tertentu energi elektron adalah tetap.
Tidak dapat menjelaskan spektrum unsur halogen. -Kelemahan Teori Atom Niels Bohr i penyimpangan untuk atom yang lebih besar daripada hidrogen. Kelemahan model atom Bohr yaitu.
Orbitalkulit elektron yang mengelilingi inti atom tidaklah berbentuk lingkaran melainkan elips.
Teori Atom Rutherford Dan Teori Atom Niels Bohr Yang Perlu Kamu Ketahui Kumparan Com
Perkembangan Teori Atom Siswapedia
Teori Atom Rutherford Dan Teori Atom Niels Bohr Yang Perlu Kamu Ketahui Kumparan Com

Teori Atom Bohr Pengertian Karakteristik Kelemahan Postulat Konsep Penting Dan Penjelasan Apayangdimaksud Com
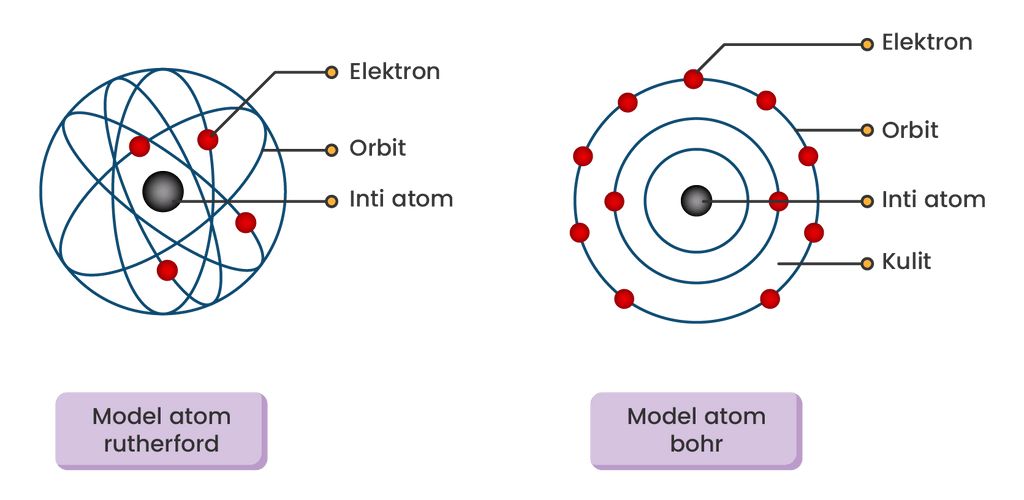
Teori Atom Rutherford Memiliki Kelemahan Tidak Dap

Teori Atom Dalton Materi Kimia

4 Teori Atom Menurut Para Ahli Dan Perkembangannya Ilmu Kimia

Komentar
Posting Komentar